4月2日,中国科学院上海营养与健康研究所詹丽杏研究组与江苏省人民医院徐骁教授、浙江中医药大学附属第一医院包海标教授、海军军医大学长海医院李刚教授合作,在国际知名学术期刊Gut在线发表了题为“Selenoprotein P Deficiency Drives Hepatocellular Carcinoma Progression via Induction of Neutrophil Senescence and Immunosuppressive Microenvironment”的研究成果。该研究首次发现肝脏肿瘤中硒蛋白P(SEPP1)将诱导肿瘤微环境中性粒细胞发生衰老样重编程,通过表观遗传修饰重塑肝癌的免疫抑制性微环境,促进肿瘤进展。该研究确认了肝癌中硒干预靶向中性粒细胞的免疫干预策略。
肝细胞癌(HCC)是全球范围内高发的恶性肿瘤,其复杂的免疫微环境是导致免疫治疗耐受的关键原因。近年研究显示中性粒细胞是肝癌微环境中重要的免疫细胞,具有高度的异质性和可塑性。尽管已有研究提示衰老样中性粒细胞具有免疫抑制功能,但其在肝癌中的分子特征及诱导机制尚不明确。流行病学研究也显示血清硒及SEPP1水平降低与肝癌风险增加密切相关,但其背后的生物学机制不明。
研究团队通过对多种小鼠肝癌模型及人肝癌样本的整合分析发现,SEPP1在肝癌组织中显著下调。利用单细胞转录组测序(scRNA-seq)技术,研究人员在肝癌组织中鉴定出了一群独特的“衰老样”肿瘤浸润中性粒细胞(TINs)。这群细胞以Cdkn1a(p21)、S100a8/9及Vegfa的高表达为特征,展现出显著的衰老相关分泌表型(SASP)。实验证明,肝脏特异性敲低SEPP1会显著增加这群衰老样中性粒细胞的比例,进而抑制CD8+T细胞的浸润与活性,促进肝癌进展。
在机制方面,研究发现肿瘤来源的SEPP1是中性粒细胞通过LRP8受体摄取硒的关键载体。当肝癌由于高氧化应激压力下SEPP1缺失时,中性粒细胞内硒代谢紊乱,导致硒化氢(H₂Se)产量不足及S-腺苷甲硫氨酸(SAM)累积。这种硒代谢稳态紊乱导致了H3K4me3组蛋白修饰的增加,从而在表观遗传水平上开启了促衰老基因及SASP相关基因(如S100a8/9)的表达,驱动了中性粒细胞的衰老样重编程表征。
在临床转化研究中,研究人员验证了机体硒补充(如硒代蛋氨酸及亚硒酸钠)能够恢复肝脏SEPP1水平,有效逆转中性粒细胞的衰老样表型,并显著增强抗PD-1免疫治疗在肝癌模型中的疗效。与机制相吻合,使用经典的衰老细胞清除药物(Senolytics)如达沙替尼联合槲皮素(D&Q)也能显著减轻SEPP1缺失导致的肿瘤负担,恢复肝癌抗肿瘤免疫细胞活性。该研究不仅阐明了微量元素硒细胞代谢与抗中性粒细胞衰老的分子纽带,也为构建基于“硒营养-免疫代谢”的肝癌综合治疗提供充实的理论依据。
中国科学院上海营养与健康研究所博士后焦佳正、已毕业博士研究生宋乐乐,以及西湖大学医学院附属杭州市第一人民医院许圣均博士为该论文的共同第一作者。中国科学院上海营养与健康研究所詹丽杏研究员、江苏省人民医院徐骁教授、浙江中医药大学附属第一医院包海标教授、海军军医大学长海医院李刚教授为共同通讯作者。该研究得到了恩施州科技局“硒与健康”项目,科技部、国家自然科学基金委等项目的大力资助,同时也获得了营养与健康所所级公共技术中心及实验动物技术平台的支持。
论文链接:https://gut.bmj.com/content/early/2026/04/01/gutjnl-2025-336422
推送单元:詹丽杏研究组、科技规划与任务处
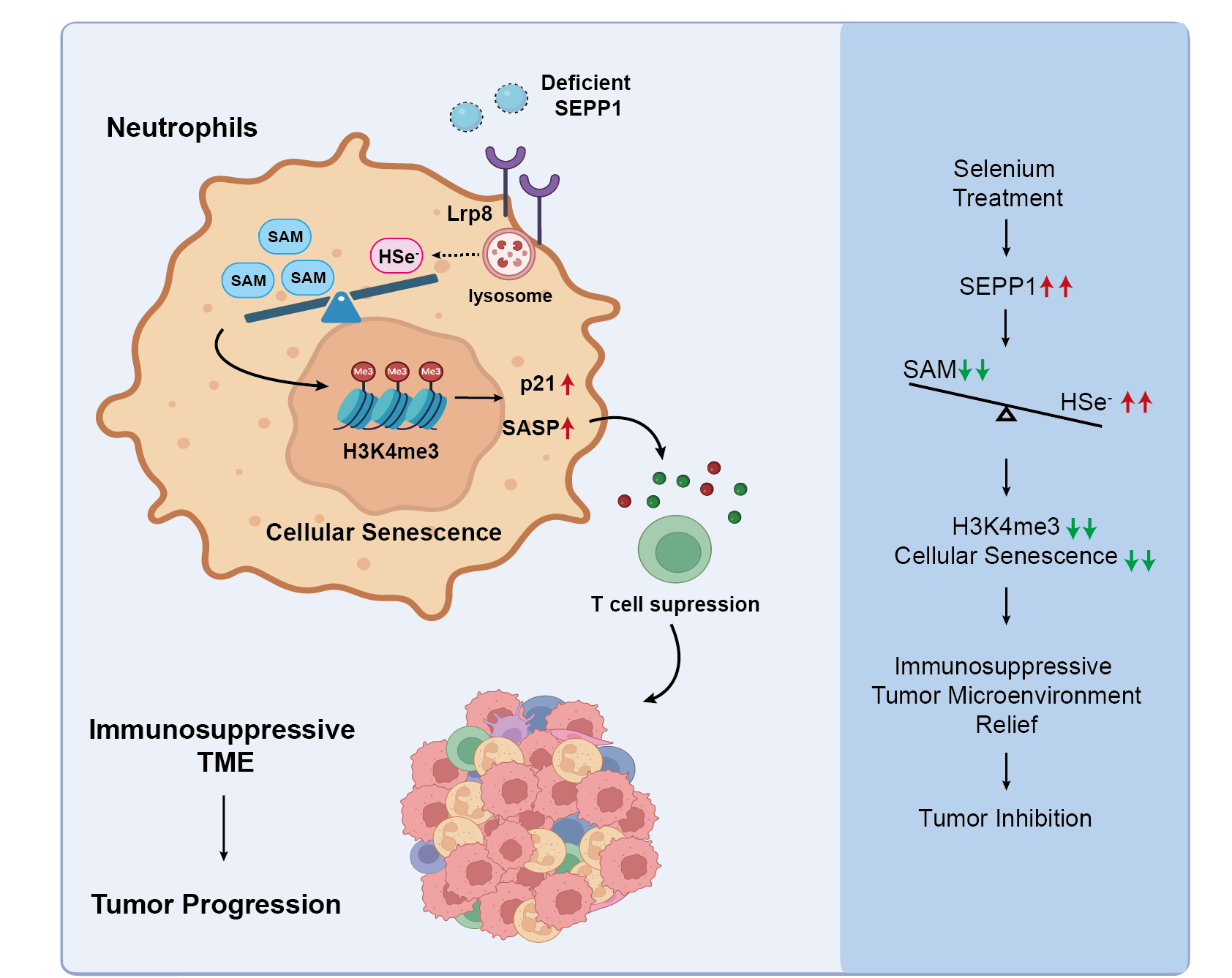
图:硒蛋白P缺乏通过诱导中性粒细胞衰老和免疫抑制微环境促进肝癌进展