4月2日,中国科学院上海营养与健康研究所王兰研究组联合多家单位,在Science Translational Medicine期刊发表题为“Site specific methylation of SRSF2P95H by SETD2 inhibits MDSCs-mediated proinflammatory niche formation in mouse models of myelodysplastic syndrome”的研究成果。该研究从表观修饰与异常剪接等层面,揭示了组蛋白甲基转移酶SETD2在骨髓异常综合征(MDS)中调控免疫抑制性骨髓微环境形成的作用及机制。研究通过动物模型验证,提出CEACAM1-4/IL-1β(CEACAM1-4:癌胚抗原相关细胞黏附分子1剪接体;IL-1β:白细胞介素-1β)靶向策略在SRSF2P95突变型MDS中的潜在应用价值。
研究团队通过分析携带SRSF2突变的MDS患者骨髓造血干祖细胞(HSPC)的单细胞测序数据,发现SRSF2突变患者的HSPC向髓源抑制性细胞(MDSC)的分化偏倚能力增加,炎性通路显著激活,同时HSPC中SETD2显著低表达且与患者预后不良密切相关。同时遗传型模型证实,SETD2缺失可加重Srsf2P95H/+小鼠的HSPC分化偏倚能力,导致MDSC异常扩增,同时形成炎症因子IL-1β高表达的炎性骨髓微环境,同时抑制杀伤性T细胞、自然杀伤性T细胞等的增殖与功能,形成免疫抑制性骨髓微环境(iBMN),显著促进MDS疾病进展。
进一步机制研究揭示,SETD2通过催化SRSF2P95H蛋白K17和K65位点的甲基化修饰来抑制SRSF2P95H突变介导的CEACAM1-4异常剪接体的增加。CEACAM1-4剪接体异常升高可激活HSPC中的JAK2-STAT3信号通路,引起细胞膜表面胱氨酸转运蛋白SLC7A11表达上调,进而导致胞内胱氨酸水平升高。胱氨酸的异常积累进一步促进炎性因子IL-1β和IL1F9的分泌,促进HSPC向多形核型髓源性抑制性细胞(PMN-MDSCs)的分化偏倚,并抑制骨髓微环境中T细胞功能,最终形成iBMN并加剧MDS疾病进展。
在此基础上,研究团队提出,靶向CEACAM1-4/IL-1β通路可显著缓解MDS中的免疫抑制性骨髓微环境并延缓疾病进展,具有潜在的临床应用价值。该研究为理解SRSF2突变型MDS的发病机制提供了新的理论依据,并为相关靶向治疗策略的开发提供了重要线索。
中国科学院上海营养与健康研究所博士后李子娟、博士生赵木英,上海市第六人民医院王柔嘉医师及海军军医大学第一附属医院刘娜助理研究员为论文共同第一作者。中国科学院上海营养与健康研究所王兰研究员、上海交通大学瑞金医院孙晓建研究员、上海市第六人民医院常春康主任及西安交通大学第一附属医院贺鹏程主任为论文通讯作者。该研究得到了科技部、国家自然科学基金委等项目的支持。该工作得到了陈竺院士、陈赛娟院士的指导,以及中山大学肿瘤防治中心血液肿瘤科梁洋主任和美国西北大学范伯格医学院刘岩教授的大力支持。
原文链接:https://doi.org/10.1126/scitranslmed.adv1065
推送单元:王兰研究组、科技规划与任务处
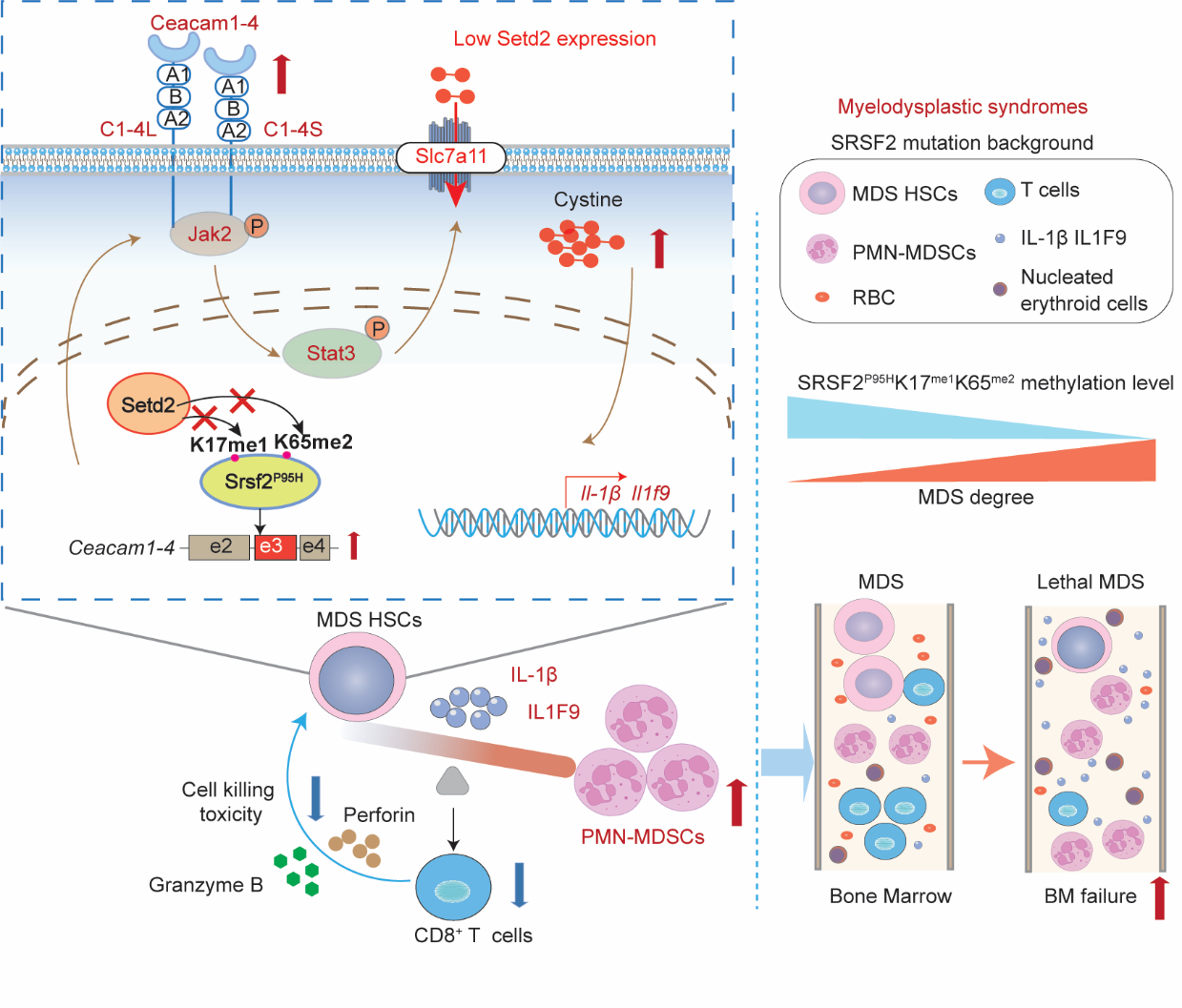
图:SETD2调控骨髓异常综合征免疫抑制微环境形成的机制及靶向策略