11月1日,国际期刊Nature communications在线发表了中国科学院上海营养与健康研究所钱友存研究组题为“Dietary nucleic acids promote oral tolerance through innate sensing pathways in mice” 的最新研究成果。该研究发现饮食来源的核酸可以在稳态条件下促进小鼠小肠中天然上皮内淋巴细胞(natural intraepithelial lymphocytes, natural IELs)的发育和维持,揭示了这群细胞在蛋白质抗原介导的口服耐受中也发挥重要调节作用,加深了我们对于天然IEL发育以及肠道免疫耐受机制的认识。
肠道是人体重要的消化吸收场所,也是最大的免疫器官。肠道菌群、免疫细胞和黏膜屏障共同筑成了肠道上皮的稳态。其中,上皮内淋巴细胞是存在于肠道黏膜上皮的一类特殊免疫细胞,它们表达不同的TCR受体以及不同组合的CD4、CD8α、CD8β等分子标记物。此外,它们在维持肠道免疫稳态、保护上皮屏障以及参与免疫应答中扮演重要角色。与传统T细胞的发育成熟机制不同,这群T淋巴细胞的发育成熟更多依赖于肠道黏膜微环境。但是关于它们是如何维持发育成熟的,目前还并不是特别清楚。目前已知诱导性IEL主要受到肠道菌群的影响,但是关于占比较多的天然IEL,它们受什么因素的调控却并不清晰。作为模式识别受体大家族(Pattern Recognition Receptors,PRRs)中的一个重要分支,核酸受体(nucleic acid receptors)在肠道黏膜中有着广泛的表达,研究人员猜想这些受体除了在外来病原菌感染中发挥作用外,是否也会在稳态条件下识别微环境中的因素,进而参与调控上皮内淋巴细胞的发育。
通过流式分析的方法,研究人员系统性分析了核酸受体及其下游重要接头蛋白缺陷的小鼠中稳态条件下IEL的发育情况,发现在MAVS和STING双缺失(MS DKO)的情况下,小鼠小肠中的两群天然IEL(TCRγδ+和TCRαβ+CD8αα+)在比例和数目均显著减少。随后,通过分析比较无菌小鼠中天然IEL的发育情况,研究人员发现这群细胞的发育并不依赖于肠道菌群。最后,通过给老鼠饲喂合成饲料,研究人员发现这群细胞的发育依赖于饮食中的核酸。机制上,研究人员发现饮食中的核酸能够通过影响肠道上皮细胞中的IL-15的表达水平来影响天然IEL的发育。
这群受食物中核酸调控的天然IEL有什么功能呢?由于口服耐受是由受食物中蛋白质抗原影响而建立的肠道免疫耐受,研究人员猜想这些IEL是不是也可以影响口服耐受。口服耐受是指食物中溶解性的蛋白质抗原摄入后,可以被肠道中的CD103+树突状细胞摄取,然后加工递呈给肠系膜淋巴结中的Treg细胞,从而促进分化出抗原特异性的Treg。当下次相同的抗原再刺激时,免疫反应往往很难发生,也就是出现了耐受。研究人员选用OVA蛋白质抗原诱导的模型,发现在MS DKO老鼠和合成饲料饲喂的老鼠中, OVA 介导的口服耐受都无法正常建立,而回补天然IEL,可以促进耐受的建立。随后,研究发现天然IEL在面对蛋白质抗原刺激的时候,可以通过分泌Tgfb1促进CD103+ DC表达整合素b8,而这个分子对于CD103+ DC促进抗原特异的Treg分化十分重要。最后,研究人员通过Tgfb1缺失的IEL 回补也证明了IEL对OVA-Treg的间接调控。
建立针对食物抗原的口服耐受对于肠道稳态的维持至关重要。其中,食物来源的蛋白质抗原在口服耐受性中起着至关重要的作用。研究人员发现,饮食中的核酸(包括RNA和DNA)可激活核酸受体传感通路以维持天然IEL,从而促进蛋白质抗原驱动的口服耐受,表明饮食核酸在建立和维持口服耐受性和肠道稳态方面发挥着关键作用。
中国科学院上海营养与健康研究所博士后杨涛为该论文的第一作者,钱友存研究员为通讯作者。该工作还受到中国科学院上海营养与健康研究所邱菊研究员、胡国宏研究员,中国科学院分子细胞科学卓越创新中心陈剑峰研究员、宋昕阳研究员以及广州医科大学冷启彬研究员的支持和帮助。
该工作得到了科技部国家重点研发计划项目、国家自然科学基金委的资助,以及中国科学院上海营养与健康研究所所级公共技术中心分析测试技术平台和实验动物技术平台的支持。
文章链接:https://www.nature.com/articles/s41467-024-53814-0#Sec10
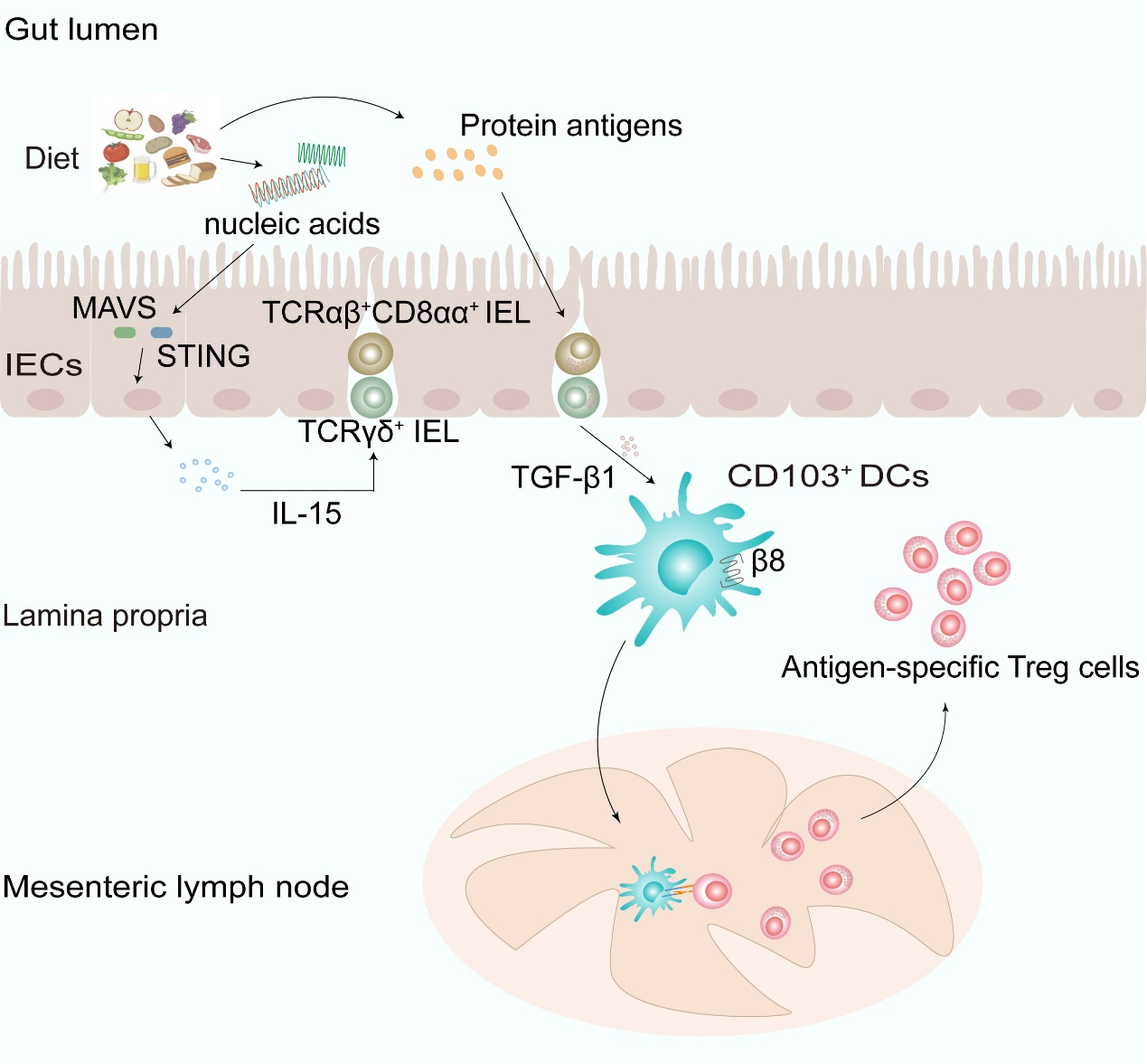
图注:饮食中的核酸通过调控小肠中天然上皮内淋巴细胞的稳态来促进口服耐受的建立