2022年4月9日,国际学术期刊JCI insight在线发表了中科院上海营养与健康研究所尹慧勇研究组题为 “Aldehyde dehydrogenase 2 and PARP1 interaction modulates hepatic HDL biogenesis by LXRα-mediated ABCA1 expression”的研究成果。该研究揭示了线粒体乙醛脱氢酶2(Aldehyde Dehydrogenase 2, ALDH2)通过直接与DNA修复酶聚腺苷二磷酸核糖聚合酶1(poly ADP-ribose polymerase, PARP1)相互作用调控转录因子肝X受体α (Liver X Receptor α, LXRα) 对ATP结合盒转运体A1(ATP-binding cassette transporter 1, ABCA1)的转录,从而影响肝脏的高密度脂蛋白(High Density Lipoprotein, HDL)的生成。
心血管疾病是全球范围内发病率和死亡率最高的疾病,动脉粥样硬化是心血 管疾病发病的重要原因之一。动脉粥样硬化疾病的发生发展与脂质代谢紊乱、氧化应激、炎症反应以及基因遗传等密切相关。脂质代谢中的胆固醇代谢一直是动脉粥样硬化的研究重点,并且临床上总胆固醇(Total Cholesterol, TC)、低密度脂蛋白(Low Density Lipoprotein, LDL)、高密度脂蛋白水平是诊断心血管疾病的重要生化指标。血液中LDL水平的升高和HDL水平的降低是心血管疾病和动脉粥样硬化的风险因素。ALDH2是人体功能性醛脱氢酶(ALDHs)家族的重要成员,在乙醛和其他醛类的代谢中起着重要作用。流行病学以及全基因组关联分析发现,携带有ALDH2 rs671突变(喝酒脸红基因)的人群具有更高的心血管疾病风险;并且ALDH2 rs671突变与血液HDL-C水平具有相关性:携带有ALDH2 rs671突变的人群HDL-C呈显著性下降趋势。由于约30-50%的东亚人群(包括中国人群)携带ALDH2rs671,因此,研究ALDH2在HDL代谢中作用与机制对有效预防和治疗心血管疾病有重要临床意义。
在本项目中,研究人员发现给予西方饮食的ALDH2敲除,ALDH2/LDLR双敲,和ALDH2 rs671敲入的小鼠血浆HDL-C显著下降,但肝脏胆固醇水平与脂质堆积增加,肝脏胆固醇外排生成HDL-C的重要蛋白ABCA1下调表达,提示肝脏ALDH2在调控HDL代谢中发挥重要作用。接着,利用非靶向高分辨质谱代谢组学发现ALDH2/LDLR双敲小鼠与LDLR敲除小鼠相比,在给予西方饮食时血清中腺苷二磷酸核糖(ADP-Ribose)水平显著升高,提示PARP1通路可能参与其中。进一步的机制研究发现:ALDH2与PARP1的入核序列结合抑制PARP1的入核,使其对LXRα的聚(ADP-核糖基)化下降,从而促进ABCA1的表达,最终增加肝脏胆固醇的外排与生成HDL。相反,ALDH2的敲除或者突变解除降低了其对PARP1入核的抑制,使LXRα的聚(ADP-核糖基)化增加,抑制ABCA1的表达,减少肝脏胆固醇的外排,从而造成血液HDL-C水平下降。PARP1的抑制剂PJ34在ALDH2敲除小鼠中可以逆转由于西方饮食引起的肝脏脂质堆积,增加ABCA1表达,升高血液HDL-C水平。结合前期的研究,在人肝脏组织中由于ALDH2 rs671突变促进其降解,造成蛋白水平降低,同样减少ALDH2对PARP1入核的抑制,增加LXRα的聚(ADP-核糖基)化,从而降低ABCA1的表达和肝脏胆固醇向血浆中的外排与HDL的生成。
综上所述,本研究阐明了肝脏ALDH2通过PARP1-LXRα-ABCA1调控HDL代谢的新机制(如图所示),为携带ALDH2 rs671突变个体的血浆HDL-C下降提供了新解释,有望为心血管疾病的预防和治疗提供潜在临床策略。尹慧勇实验室长期关注脂代谢与心血管疾病,前期研究发现了ALDH2在巨噬细胞中调控泡沫细胞的形成(J Clin Invest 2019;129:252-267),以及肝细胞中影响胆固醇从头合成的分子机制(Redox Biol 2021;41:101019)。
中科院上海营养与健康研究所博士研究生李露晓为该论文的第一作者,尹慧勇研究员为通讯作者。该工作得到了复旦大学附属中山医院孙爱军教授、上海科技大学仓勇教授、武汉大学宋保亮教授、中科院分子细胞科学卓越创新中心李伯良研究员以及加拿大Alberta大学章大卫教授的大力支持。此课题得到了国家自然基金、基金委重大研究计划、基金委外国资深学者研究基金及科技部重点研发计划项目的资助,同时也得到了中国科学院营养与健康研究所公共技术平台与动物平台的大力支持。
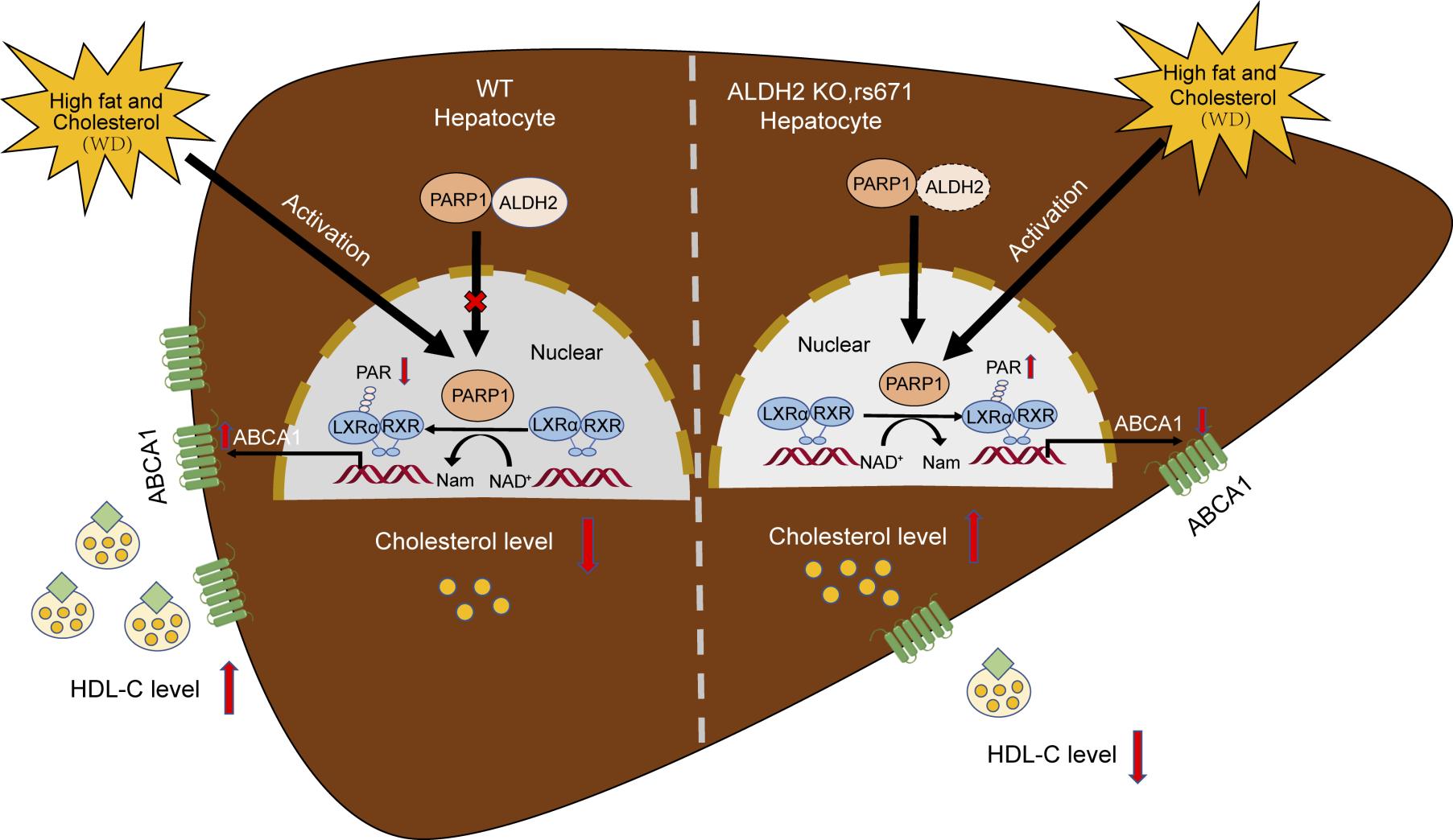
图:ALDH2通过PARP1调节HDL-C代谢的模式图
原文链接:https://doi.org/10.1172/jci.insight.155869