2023年5月4日,国际学术期刊Cell Research在线发表了中国科学院上海营养与健康研究所胡国宏研究组题为“SCUBE2 mediates bone metastasis of luminal breast cancer by modulating immune-suppressive osteoblastic niches”的最新研究成果,阐明了分泌蛋白SCUBE2在乳腺癌骨转移过程中的作用、机理及临床应用价值。
乳腺癌位列女性新发癌症之首,发生远端转移是造成乳腺癌高死亡率的主要原因。乳腺癌的转移器官有骨、肝、脑、肺等,其中骨是最常见的转移位点。临床发现乳腺癌转移有明显的器官倾向性,骨转移主要发生在雌激素受体(ER)阳性的管腔型乳腺癌(LBC)中。与其他亚型相比,LBC整体预后较好,向内脏器官的转移风险较低,却极易发生骨转移,导致这种倾向性的机制并不清晰。目前大多数乳腺癌骨转移研究基于三阴型乳腺癌模型展开,关注的是由破骨细胞介导的晚期溶骨性骨转移,但相应的药物并未取得较好的临床疗效。报导的骨转移促进因子,如CXCR4,MMP1,IL6等,也在三阴乳腺癌中表达上调,无法解释LBC的骨转移倾向性。
胡国宏研究组发现肿瘤分泌的SCUBE2是介导LBC骨转移倾向性的重要因子,可作为乳腺癌骨转移风险的血清学标记和骨转移治疗的新靶点。首先基于大规模公开临床数据分析,筛选得到在LBC中特异性表达上调的分泌蛋白SCUBE2,并在多种小鼠模型中验证了SCUBE2对骨转移的促进功能。机制研究表明SCUBE2受到LBC细胞中特异性激活的ER信号调控,并通过促进肿瘤细胞释放SHH,激活成骨前体细胞中Hedgehog信号,从而诱导成骨分化。成骨细胞大量释放COL1,通过COL1-LAIR1-SHP1轴抑制NK细胞的激活,从而解除NK细胞对癌细胞的免疫监视。使用FDA批准的Hedgehog信号抑制剂Sonidegib可以显著抑制乳腺癌骨转移的发生。此外,研究组开发了一株SCUBE2中和抗体,该抗体可显著阻断SCUBE2的功能,在多个乳腺癌骨转移模型中均表现出良好的骨转移治疗效果。
综上,这项研究阐明了SCUBE2调控乳腺癌骨转移的新机制,并支持了其在临床诊断中的意义以及靶向SCUBE2的骨转移治疗策略。而SCUBE2在LBC中的特异表达以及其功能对成骨细胞的依赖性,解释了LBC的骨转移倾向性。
中国科学院上海营养与健康研究所博士后吴秋瑶为该论文的第一作者。中国科学院上海营养与健康研究所胡国宏研究员和山东大学齐鲁医院杨其峰教授为该论文的共同通讯作者。该工作得到了复旦大学肿瘤医院邵志敏教授和江一舟教授,以及中国科学院上海营养与健康研究所秦骏研究员的合作支持。研究项目得到了科技部、国家自然科学基金委、中国科学院和上海市科委的资助,以及上海营养与健康研究所所级中心公共技术平台的支持。
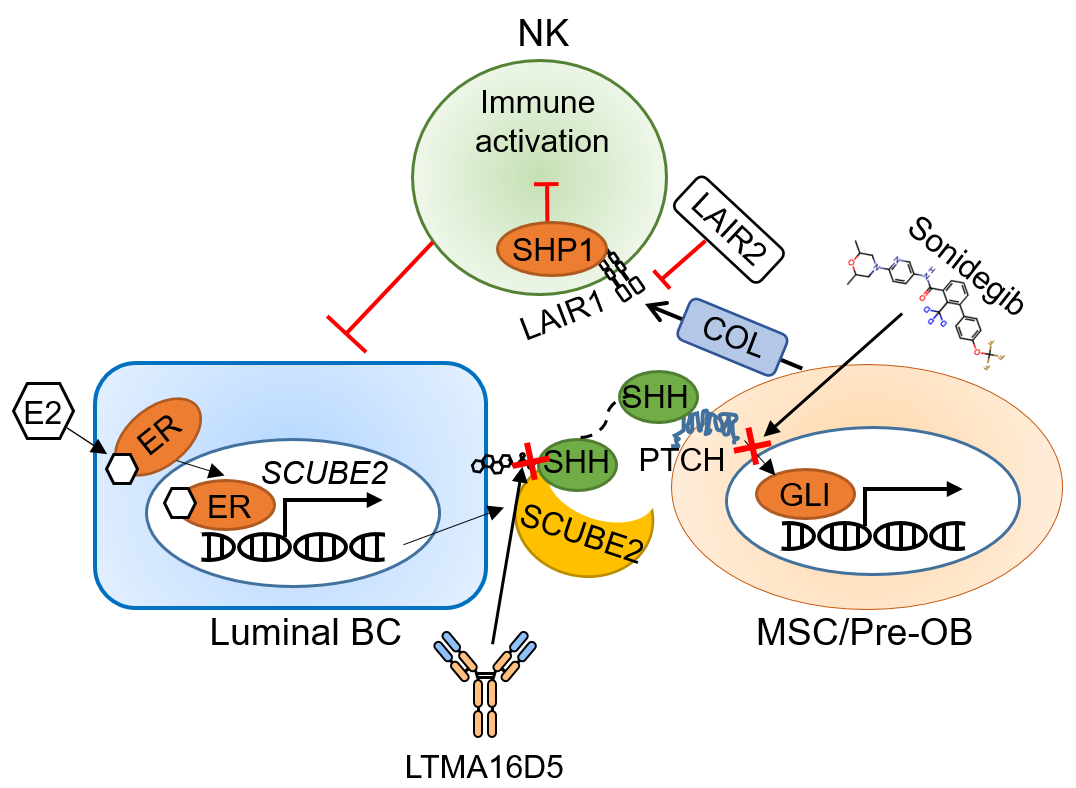
SCUBE2调控免疫抑制性成骨细胞及乳腺癌骨转移的功能机制图